



微环境的改变或许是成体干细胞衰老的主要原因。德国科学家研究发现:在毛发的再生过程中,低氧会促进组织微环境中的谷氨酰胺代谢转变为糖酵解,从而维持毛囊干细胞的数量。
成年人的世界没有容易的事,除了脱发。在日常生活中,皮肤和毛囊会不断被各种环境因素损害,比如紫外线辐射。据估计,一个成年人平均每天脱落5亿个细胞和100根头发。与此同时,受损的皮肤和毛囊会不断地被移除和更新,而毛囊干细胞则在这一过程中发挥重要作用。
根据国家卫健委发布的脱发人群调查数据,中国已经有超过2.5亿人正饱受脱发的摧残。也就是说,平均每6人里就有1人头秃。

毛囊干细胞的基本功能
毛囊干细胞(hair follicle stem cells,HFSC)是毛囊中的原始细胞,人的头发和体毛都是从毛囊中生长出来的。不过,负责生发的毛囊干细胞通常处在休眠状态,但会在新一轮生发周期中迅速活化分裂。当相邻部位受到损伤后,毛囊干细胞可从原定位的隆突部中迁出并参与损伤部位修复。
毛囊是毛发的基本单位,而毛发是由毛囊内的细胞生长分化而来。每根毛囊里面住着一群毛囊干细胞,提供新的细胞给生长中的毛囊。人毛囊干细胞属于成体干细胞的一种,具有成体干细胞的共性。人体的许多组织功能依赖于干细胞的健康活动。因此,干细胞的受损或数量减少会导致人的衰老。
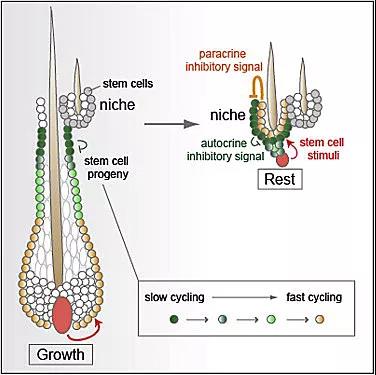
毛囊干细胞
有趣的是,当毛发开始生长时,毛囊干细胞被激活产生祖细胞,随后分化为其子细胞(毛囊外根鞘细胞,Outer root sheath,ORS)以提供细胞毛囊生长所需的营养,而当毛发生长处于退行期时,部分外根鞘前体细胞会去分化形成新的毛囊干细胞。但为什么会这样,大家对其中机制知之甚少。

谷氨酰胺代谢控制毛囊干细胞命运
近日,德国科隆大学和马普所衰老生物学研究所的科学家们在Cell Metabolism上发表了题为Glutamine Metabolism Controls Stem Cell FateReversibility and Long-Term Maintenance in the Hair Follicle的最新研究成果。
他们发现:毛囊干细胞可以通过响应组织中的低氧浓度而切换其代谢状态(由谷氨酰胺代谢转变为糖酵解代谢),增强外根鞘祖细胞向毛囊干细胞转化,减少毛囊干细胞的消耗。
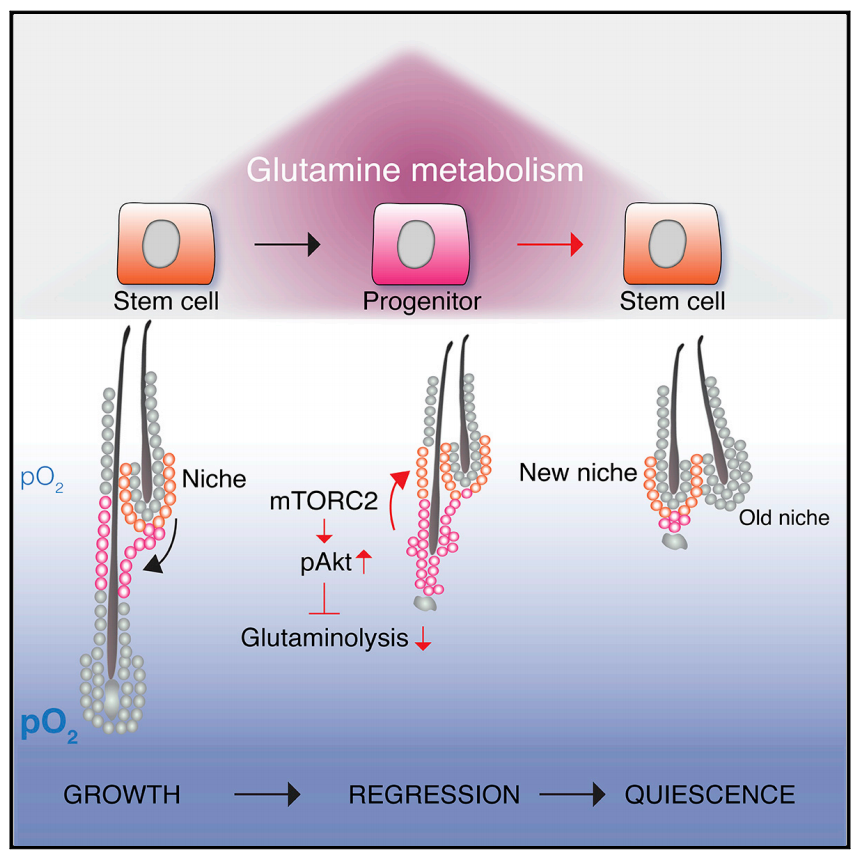
毛囊干细胞调控机制研究
那么,到底是什么使得毛囊干细胞在功能上不同于其子细胞,带着这个问题,研究小组探究了这两者的转录组和代谢谱。有趣的是,他们发现毛囊干细胞与其子细胞(ORS祖细胞)具有不同的代谢特征。
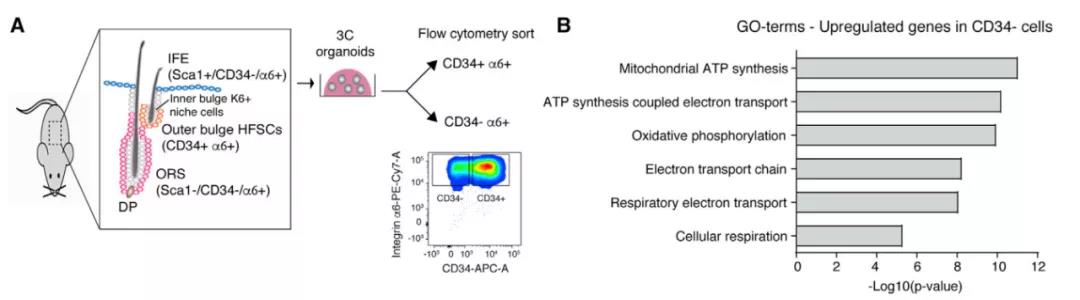
毛囊干细胞和子细胞具有不同的代谢特征
ORS祖细胞中参与氧化磷酸化(OXPHOS)的基因高度表达,三羧酸(TCA)循环中的代谢产物也明显增加,而毛囊干细胞中的线粒体明显较少,且线粒体相关基因的表达水平也较低。毛发生长初期,ORS区域的氧化程度比毛囊更高,与处于激活状态的毛囊干细胞一致。
研究发现,低氧增加会触发毛囊干细胞的增加,2%的氧气浓度即可增强ORS祖细胞返回毛囊干细胞状态。其机制是,低氧会促进谷氨酰胺代谢转变为糖酵解,从而增加依赖于低氧糖酵解提供能量的毛囊干细胞。
毛囊干细胞调控机制
为了进一步确定调控毛囊干细胞的机制,研究人员对代谢基因的上游调控因子进行鉴定,发现mTORC2(mTOR信号转导调节细胞的生长,能量和氧气消耗等过程)的重要组成蛋白之一Rictor可能也参与调控毛囊干细胞的调控。
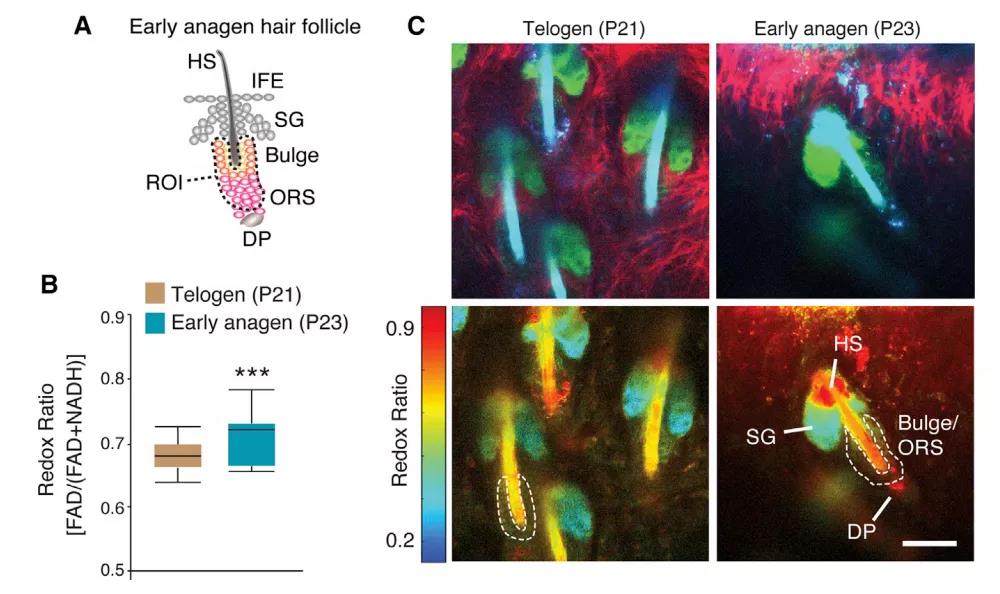
进入毛囊生长期,毛囊干细胞氧化增加
研究团队发现,毛囊干细胞的消耗是由于代谢稳态的丧失。实际上,毛囊干细胞适宜在低氧环境中。毛囊干细胞更倾向于使用糖酵解代谢,而非谷氨酰胺代谢提供能量。这种代谢切换是由低氧环境和Rictor信号引发的。毛囊干细胞的‘命运可逆性’,需要满足的条件就是从谷氨酰胺代谢与糖酵解代谢之间的切换。
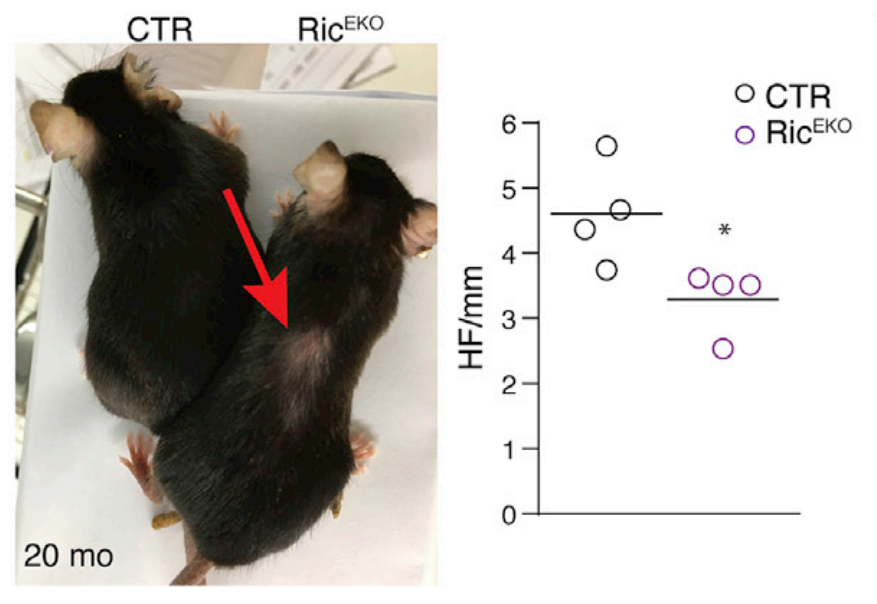
Rictor敲除小鼠模型表现出脱发特征
通过构建Rictor敲除小鼠进行验证,观察到缺少Rictor的小鼠显著延迟了毛囊的再生和循环,毛囊干细胞数量减少。随着年龄的增长,这些老鼠出现了年龄诱导性脱发和毛囊干细胞的耗竭。
文末小结
该研究的通讯作者德国科隆大学的皮肤科医学教授Sabine Eming 说,令人兴奋的是,我们发现使用谷氨酰胺酶抑制剂能够恢复Rictor缺陷型小鼠的毛囊干细胞功能,这意味着修饰代谢途径可能是增强组织再生能力的一种有效方式。
未来的主要研究目标是如何将这些研究转化应用于临床,以防止毛囊老化,让治疗脱发成为可能。
参考资料:
[1]Kim CS. etal;Glutamine Metabolism Controls Stem Cell Fate Reversibility and Long-Term Maintenance in the Hair Follicle. Cell Metab. 2020 Oct 6;32(4):629-642.e8.
——文章来源:干细胞者说